Una base o alcali en química es un tipo de compuesto que cuando se disuelve en agua libera iones negativos hidroxilo OH- o acepta un protón H+. En contraste, un ácido al disolverse en agua libera o dona iones positivos de hidrógeno o protones H+.
Por lo general, una base se representa como BOH, donde B+ es el metal o radical que se une al hidroxilo OH-:

Cuando una base se disuelve en agua obtenemos una solución básica o alcalina. Estas soluciones las podemos identificar al medir su pH, una medida de la acidez. Las soluciones básicas o alcalinas tienen un pH mayor a 7.
Cuando ácidos y bases se juntan, se produce una reacción de neutralización, esto es, el ácido anula o contrarresta la base.
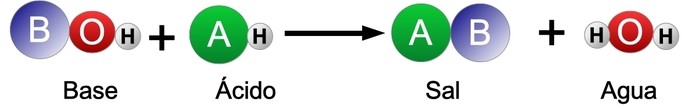
En la reacción entre un ácido y una base se forma una sal y agua, que se puede representar de la siguiente manera:
Características de las bases
- Tornan azul el papel de tornasol.
- Sensación resbaladiza o jabonosa.
- Pueden ser sólidos o líquidos.
- Reaccionan con ácidos formando sales y agua.
- Se disocian en agua liberando iones.
- Pueden ser bases fuertes, cuando se disocian fácilmente, o bases débiles, cuando la disociación es menor.
Ejemplos de bases
Entre las bases químicas que más se usan en el día a día podemos mencionar:
- el amoniaco NH3, presente en productos de limpieza;
- la leche de magnesia Mg(OH)2, en tratamiento contra la acidez estomacal;
- el hidróxido de sodio NaOH, en limpiadores de hornos;
- el hidróxido de calcio Ca(OH)2 que se usa en construcción;
- el hidróxido de potasio KOH, en baterías alcalinas;
- el hidróxido de bario Ba(OH)2, como pesticida;
- el bicarbonato de sodio NaHCO3., en productos alimenticios.
Vea también: